炎症和疼痛是人体面对损伤或感染时发出的警示信号,但在持续或过度反应的状态下,它们可能演变为影响生活质量的健康问题。随着医学发展,天然草本成分与现代药物技术的结合,为消炎镇痛提供了更安全有效的解决方案。
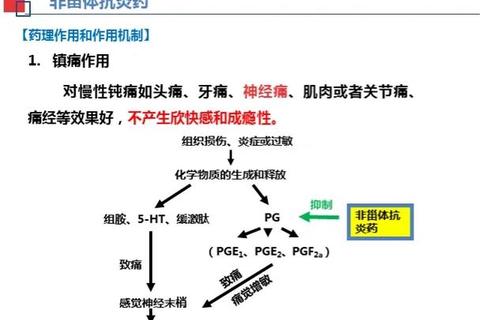
当机体遭遇外界刺激(如细菌感染、外伤)或内部失衡(如代谢异常)时,免疫系统会释放组胺、前列腺素、白三烯等炎症介质,引发血管扩张、组织水肿和神经敏感。这一过程中,环氧酶(COX)、肿瘤坏死因子(TNF-α)等关键蛋白的过度激活是导致红肿热痛的核心因素。值得注意的是,慢性炎症可能引发纤维化、器官功能障碍等严重后果,例如关节炎患者的关节破坏或肠炎患者的肠道屏障损伤。
传统草药通过多靶点协同作用调节炎症网络,其优势在于成分多样性带来的综合效应:
1. 延胡索:主要活性物质延胡索乙素能抑制脊髓背角D2受体,阻断痛觉信号向大脑传递,同时调节下丘脑-垂体-肾上腺轴,降低应激激素水平。其抗炎作用还体现在抑制NLRP3炎性小体,减少IL-1β等促炎因子释放。
2. 大黄:含有的蒽醌类化合物通过抑制COX-2和5-脂氧合酶(5-LOX)双重通路,减少前列腺素和白三烯生成。研究表明,大黄素可降低CVB4病毒复制效率,对病毒性心肌炎引发的胸痛有显著缓解。
3. 连翘与黄芩:连翘苷通过阻断TLR4信号通路抑制炎症级联反应,而黄芩苷可调节Th17/Treg细胞平衡,在类风湿性关节炎模型中显示出关节保护作用。
这些草本成分的独特之处在于:既可直接拮抗炎症介质(如阻断COX酶活性),又能调节免疫细胞功能(如巨噬细胞极化),还能通过抗氧化减少组织氧化损伤。
传统草药制剂面临生物利用度低、血药浓度波动大的挑战。现代药剂学通过以下技术突破实现精准治疗:
1. 胃滞留系统:采用羟丙甲纤维素等亲水凝胶材料,使含大黄提取物的片剂在胃内膨胀滞留,持续释放蒽醌类物质以缓解胃黏膜炎症。
2. 微囊化包埋:将延胡索乙素包裹于聚乳酸-羟基乙酸(PLGA)微粒中,通过控制聚合物降解速度实现72小时缓释,避免血药浓度峰谷波动导致的嗜睡副作用。
3. pH响应型纳米粒:针对肠道炎症部位pH升高的特性,设计壳聚糖/海藻酸钠复合载体,确保连翘黄酮在结肠靶向释放,局部药物浓度提高3倍以上。
临床试验数据显示,采用缓释技术的复方延胡索制剂可使骨关节炎患者每日服药次数从3次减至1次,疼痛评分降低40%且胃肠道不良反应发生率下降60%。
草本成分与缓释技术的结合并非简单叠加,而是形成三级协同网络:
1. 时空协同:速释组分(如黄芩苷)快速抑制急性炎症反应,缓释组分(如延胡索生物碱)持续调节疼痛中枢,形成“即时阻断+长效维持”效应。
2. 代谢协同:大黄酸在肝脏转化为活性更强的芦荟大黄素,缓释系统通过维持肝酶代谢速率稳定,避免活性成分过早失活。
3. 系统协同:纳米载体表面修饰的RGD肽可靶向炎症部位整合素受体,同时搭载的姜黄素与连翘苷形成自由基清除-免疫调节双重通路。
1. 家庭护理方案
2. 就医指征判断
出现以下情况需立即就诊:
3. 特殊人群调整
基因测序技术的进步正在推动个性化给药系统的诞生。通过检测患者的COX-2基因多态性,可定制含特定比例塞来昔布与姜黄素的缓释胶囊。3D打印技术则能制造出芯壳结构药片,实现昼夜节律适配的药物释放——例如日间释放抗炎成分,夜间释放镇痛成分。
这种融合了千年草药智慧与现代工程技术的治疗体系,不仅重新定义了炎症管理范式,更开创了精准医学时代下“天然-合成”协同治疗的新纪元。患者在获得更好疗效的真正实现了治疗过程的人性化与智能化。