消化性溃疡是胃酸和消化液侵蚀胃或十二指肠黏膜形成的慢性疾病,全球患病率高达5%~10%。其典型症状包括上腹灼痛、餐后饱胀,严重时可能导致消化道出血甚至穿孔。随着新型药物剂型和幽门螺杆菌根除方案的突破,患者康复率显著提升,但合理用药仍是关键。

发病机制
胃黏膜防御机制与胃酸攻击失衡是核心病理。幽门螺杆菌感染(占十二指肠溃疡70%)和非甾体抗炎药(NSAIDs)是主要诱因。近年研究显示,长期使用质子泵抑制剂(PPI)可能通过改变肠道菌群增加复发风险。
典型症状
• 疼痛特征:剑突下灼痛,十二指肠溃疡常表现为“饥饿痛”,进食缓解;胃溃疡则可能餐后加重
• 伴随症状:反酸、嗳气、恶心,约30%患者出现夜间痛醒
• 危险信号:呕血、黑便、突发剧烈腹痛提示出血或穿孔,需立即就医
特殊人群差异
• 孕妇:妊娠后期胃痛可能与子宫压迫有关,但需警惕溃疡恶化。避免使用含铋剂的黏膜保护剂,PPI中兰索拉唑属于B类用药
• 儿童:症状不典型,多表现为食欲减退和生长迟缓,诊断依赖胃镜检查
初筛手段
• 尿素呼气试验:幽门螺杆菌检测首选,准确率>95%
• 粪便潜血试验:筛查无症状出血
确诊金标准
胃镜检查可直接观察溃疡形态(A期活动性溃疡或S期瘢痕),必要时取活检排除恶性病变。新兴的胶囊内镜适用于不耐受传统检查者。
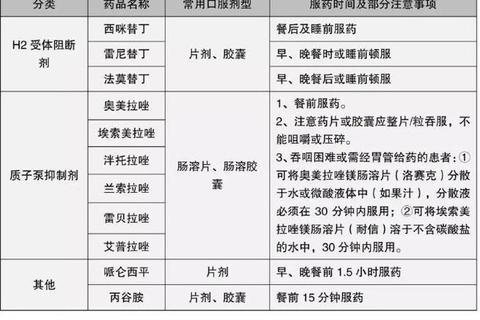
质子泵抑制剂(PPI)
• 作用机制:阻断H+/K+-ATP酶,抑酸效果可持续20小时
• 代表药物:奥美拉唑、雷贝拉唑(起效最快)
• 疗程:十二指肠溃疡4-6周,胃溃疡6-8周
• 注意事项:长期使用可能增加骨折和肠道感染风险,建议最低有效剂量维持
H2受体拮抗剂(H2RA)
• 优势:适用于轻症或PPI不耐受者,雷尼替丁已从市场撤回,法莫替丁成为优选
• 局限性:易产生耐药性,连续使用2周后抑酸效果下降50%
• 铋剂:枸橼酸铋钾可在溃疡面形成蛋白铋复合物,兼具抑制幽门螺杆菌作用
• 前列腺素衍生物:米索前列醇对NSAIDs相关溃疡效果显著,但孕妇禁用
• 新型制剂:胃漂浮片延长药物滞留时间,复方制剂(如泮托拉唑+替硝唑)提高依从性
2024年《京都共识》推荐:
markdown
1. PPI标准剂量(如艾司奥美拉唑20mg bid)
2. 阿莫西林1g bid(青霉素过敏换四环素)
3. 克拉霉素500mg bid 或 左氧氟沙星500mg qd
4. 铋剂220mg bid
疗程14天,根除率可达90%
耐药菌株地区可选用沃诺拉赞替代PPI,该药物通过竞争性抑制钾离子通道增强抑酸效果。
出血性溃疡
• 内镜下止血(热凝或钛夹)联合大剂量PPI静脉注射(如艾司奥美拉唑80mg冲击后8mg/h维持)
• 输血阈值:血红蛋白<70g/L或出现休克征象
难治性溃疡
• 检查是否合并胃泌素瘤(血清胃泌素>1000pg/ml)
• 换用伏诺拉生(P-CABs)每日1次,该药物不受进食影响且无夜间酸突破现象
复发预防
• NSAIDs使用者:联合米索前列醇或高剂量PPI
• 幽门螺杆菌根除后年复发率<5%,未根除者达60%
饮食调整
• 宜食:高蛋白(鱼、豆腐)、维生素U(卷心菜汁)
• 禁忌:咖啡因、酒精、高盐腌制品(损伤黏膜且促进幽门螺杆菌定植)
监测随访
• 治疗结束4周后复查幽门螺杆菌
• 胃溃疡患者治疗后6-8周复查胃镜排除恶性转化
• 微生态调节:益生菌(如布拉氏酵母菌)辅助治疗可降低抗生素相关性腹泻发生率
• 中医药整合:黄芪建中汤联合西药提高愈合质量,但需避免含重金属成分的偏方
• 基因检测:CYP2C19基因多态性检测指导PPI个体化用药正在临床试验阶段
特别提醒:出现体重骤减、吞咽困难或贫血症状时,务必排除胃癌可能。夜间外卖习惯人群应注意幽门螺杆菌交叉感染风险,建议家庭分餐制。